تاریخ دقیق اختراع اولین فشفشه مشخص نیست. با این حال، فشفشه به شکل فعلی آن بیش از 100 سال پیش توسط فرانتس جاکوب ولتر (1) اختراع شد. ترکیب شیمیایی دقیق اولین جرقه در پتنت این مخترع ثبت نشده است.
فشفشه ها از زمان اختراع خود، مردم را با جرقه های جذاب مجذوب خود کرده اند. علاوه بر استفاده از فشفشه در زمان کریسمس و در شب سال نو، از فشفشه برای تزئین غذا در جشن تولد یا جشن عروسی استفاده می شود. با این حال، به دلیل مواد شیمیایی موجود در این ترکیبات، فشفشه ها می توانند برای سلامتی خطرناک باشند (2).
فشفشه های معمولی از نیترات باریم به عنوان اکسید کننده استفاده می کنند بنابراین، بلع محصولات احتراق فشفشه، حاصل از گرد و غبار ناشی از جرقه بر روی غذا و استنشاق دود جرقه می تواند برای سلامتی مضر باشد. در این مقاله روشی جدید و ساده از تولید فشفشه به روشی آسان با سمیت پایین ارائه شده است.
در حال حاضر در فشفشه های معمولی نیترات باریم به عنوان اکسید کننده استفاده می شود که سمیت بالایی دارد. جایگزینی این اکسید کننده با نیترات استرانسیم و همچنین کاهش وزن مخلوط نسبت به مخلوط حاوی نیترات باریم، سبب شده تا فشفشه ساخته شده کمتر خطرناک بوده و سمیت پایین تری داشته باشد. معمولا فشفشه ها از پنج جزء اصلی تشکیل شده اند (3):
- اکسید کننده: منبع اکسیژن برای اکسیداسیون فلزات
- آهن: برای ایجاد جرقه های فشفشه
- آلومینیوم و منیزیم: به صورت پودر یا غبار برای تسریع واکنش
- بایندر: آرد، نشاسته، دکسترین یا مواد شیمیایی مشابه با مخلوط شدن با آب تبدیل به چسب می شوند و در نتیجه مواد تشکیل دهنده فشفشه را در کنار هم نگه می دارند.
- ماده حامل: سیم آهن، مس یا فولاد
علاوه بر این، معمولاً اجزای دیگری مانند زغال سنگ یا شکر نیز برای اطمینان از یکنواختی در بعضی موارد استفاده می شود.
معمولا برای نگه داشتن مواد به سیم فولادی در حین احتراق از بوراکس استفاده می شود (4).
از آنجایی که نیترات استرانسیوم در آب حلالیت بیشتری نسبت به نیترات باریم دارد، مخلوط جدید با دست به راحتی به دور مفتول (حامل) خم میشود.
واکنش هایی که در هنگام سوختن فشفشه انجام می شود را میتوان به صورت زیر فرض کرد:
![]()
Mدر تمام معادلات واکنش نماینده یک کاتیون فلزی دو ظرفیتی است، مانند Ba2+ یا Sr2+ است.
پودر آهن با اکسید کننده واکنش می دهد. این اکسیداسیون جرقه های معمولی یک فشفشه را ایجاد می کند که به رنگ سفید تا زرد است. اندازه ذرات آهن و محتوای کربن آن ها بر روی الگوی جرقه تاثیر می گذارد. برای دستیابی به یک الگوی جرقه خوب، مخلوط پودری 149-44 میکرومتر (مش 100 تا مش 325) توصیه می شود. برای به دست آوردن جرقه ها، که می تواند در تصاویر به عنوان ستاره تشخیص داده شود، نسبت کربن 1-2٪ ضروری است (5). معادله واکنش برای اکسیداسیون پودر آهن با اکسید کننده به صورت زیر است:
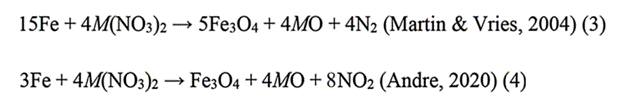
آلومینیوم:
اکسیداسیون آلومینیوم عنصری مقادیر زیادی انرژی آزاد می کند. جرقه های بدون آلومینیوم فقط می درخشند و هیچ جرقه پروازی ندارند. با توجه به مقدار زیادی انرژی آزاد شده در طی اکسیداسیون آلومینیوم، نسبت آن در تولید یک فشفشه کم خطر باید تا حد امکان کم باشد. سطح گرد و غبار آلومینیوم نسبت به پودر آلومینیوم مساحت بیشتری دارد و بنابراین سریعتر واکنش نشان می دهد. به همین دلیل، با استفاده از گرد و غبار آلومینیوم به جای پودر آلومینیوم، نسبت آلومینیوم تنها 5.7 درصد در مخلوط برای ایجاد یک الگوی جرقه خوب کافی است. علاوه بر این، فشفشه های با گرد و غبار آلومینیومی الگوی جرقه همگن تری نسبت به جرقه های با پودر آلومینیوم ایجاد می کنند. بهترین اندازه ذرات برای گرد و غبار آلومینیوم، ذرات کوچکتر از 45 میکرومتر (مش 325) است. چندین واکنش آلومینیوم با اکسید کننده در مقالات شرح داده شده است، به عنوان مثال:
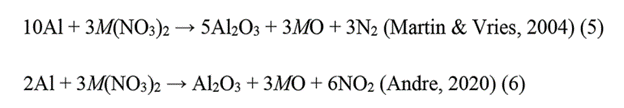
منیزیم:
سومین فلزی که معمولاً در فشفشه ها استفاده می شود منیزیم است. مشابه آلومینیوم، دمای شعله فشفشه را افزایش می دهد.
بایندر:
در فشفشه های تجاری، از دکسترین به عنوان بایندر استفاده می شود. با این حال، برای ساخت فشفشه دستی که به راحتی سیم در آن فرو رود و مواد در اطراف با دست خمیده شود از نشاسته غذایی، نشاسته محلول در آب سرد، چسب و آرد استفاده می شود.
از یک طرف، نشاسته محلول در آب سرد دارای نیروی چسبندگی خوبی است و از طرف دیگر، برای یک جرقه با 1.75 گرم مواد قابل احتراق، تنها به مقدار کمی آب (شش قطره یا 0.3 میلی لیتر) در مخلوط جرقه نیاز دارد. به این معنی که می تواند به سرعت خشک شود. بنابراین، جرقه ها پس از تنها 2 ساعت در کوره خشک کردن آماده استفاده هستند.
حامل:
برای تولید فشفشه به حامل نیاز است. فشفشه های موجود در بازار از پوشش مسی استفاده می کنند. سیم فولادی مس تضمین می کند که گرما در امتداد سیم هدایت می شود تا فشفشه به خوبی بسوزد. قطر بهینه سیم فولادی 0.8 میلی متر برای جرقه زنی با ترتیب زیر است.
مواد و تجهیزات:
نیترات استرانسیم، پودر آهن و نشاسته محلول در آب سرد را می توان از فروشنده های مواد شیمیایی استاندارد خریداری کرد.
علاوه بر این، یک سیم فولادی با ضخامت 0.8 میلی متر، یک کاردک، دو بشر 50 میلی لیتری، یک سرنگ 1.0 میلی لیتری، یک خشک کن و یک ترازوی دقیق مورد نیاز است.
ساخت فشفشه:
برای تولید یک فشفشه، مواد شیمیایی زیر مورد نیاز است (6):
-0.85 گرم نیترات استرانسیم
-0.1گرم فلکس آلومینیومی (مش 325)
-0.6 گرم پودر آهن (98٪، مش 100 تا 325)
-0.2گرم نشاسته محلول در آب سرد
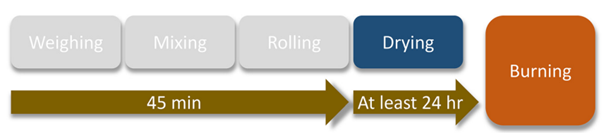
این مواد شیمیایی در حالت خشک مخلوط می شوند تا پودری همگن تشکیل شود. پنج تا شش قطره آب مقطر (حدود 0.3 میلی لیتر) به مخلوط شیمیایی اضافه می شود و مخلوط با کاردک همزده می شود تا به یک توده چسبناک تبدیل شود. پس از این، باید از دستکش های محافظ استفاده کرد تا مخلوط به شکل استوانه ای درآید. یک سیم فولادی به طول تقریبی 25 سانتی متر به شکل استوانه ای فشار داده می شود و سپس دوباره با مخلوط پوشانده و با دست رول می شود. باید تا حد امکان مواد را بطور یکنواخت قرار داد.

فشفشه به صورت عمودی در یک گلدان سفالی پر از ماسه قرار می گیرد و به مدت 24 ساعت در هوا یا به مدت 2 ساعت در دمای 70 درجه سانتی گراد در کوره خشک کن خشک می شود.

لطفا درصورت اجرای آزمایش مواظب ایمنی کار باشید.
شرکت اکسیرسازان نیک اندیش، تولید کننده و تامین کننده تخصصی مواد شیمیایی، جهت ارائه محصولات با کیفیت در خدمت شما می باشد. برای کسب اطلاعات بیشتر با ما در تماس باشید.
منابع:
- Welter, F. J. (1907). Welter, Franz Jacob, AT000000035606B
- Helmenstine, A. (2018). Are sparklers safe on cakes? Sparklers look great but present safety hazards. New York: ThoughtCo. https:// www.thoughtco.com/are-sparklers-safe-on-cakes-607432 [Accessed 21 Dec 2020]
- Keeney, A., Walters, C., & Cornelius, R. (1995). Making sparklers: An introductory laboratory experiment. Journal of Chemical Education, 72(7), 652–653
- Bast, V. (2013). Warenprobe: Wie eine Wunderkerze entsteht: Product sample: How a sparkler is made. Hamburg: Impulse. https://www.impulse.de/leben/oh-wunder/2011512.html#4 [Accessed 21 Dec 2020]
- Shimizu, T. (2010). Fireworks: The art, science and technique (4th ed.). Midland, Tex.: Pyrotechnica Publications
- M. Scheid et al.: The production of less harmful and less toxic sparklers in an experiment for school students , Chemistry Teacher International 2021; 3(3): 285–294